第32回:熱化学方程式②【化学反応と熱の出入り】
では、C(黒鉛)を不完全燃焼させてCO(気)にしたのち、さらに燃焼させてCO2(気)にすると、発生する熱量の総和はどうなるでしょうか。
C(黒鉛)をCO2(気)にするという意味で、エネルギーの差は変わりませんから、放出されるエネルギーの総和はC(黒鉛)を燃焼させてCO2(気)にしたときと同じになります。つまり熱量の総和は、C(黒鉛)の燃焼熱と同じです。
実際に、CO(気)の生成熱は111KJ/mol、CO(気)の燃焼熱は283KJ/molです。この2つの和をとると394KJになりますから、確かにCO2(気)の燃焼熱と同じになりますね。これをエネルギー図にすると、下図のようになります。
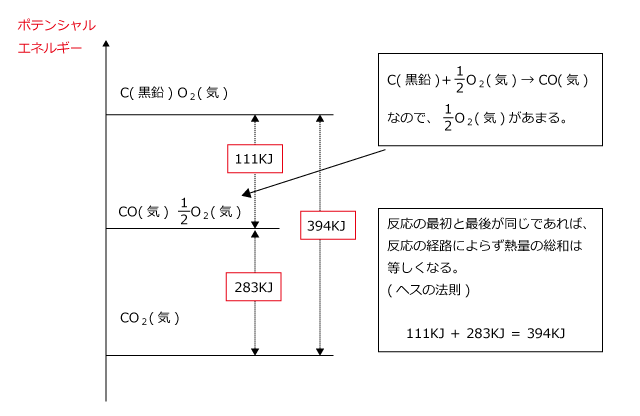
このように、反応の最初と最後の状態が同じであれば、反応の経路によらず、生じる熱量の総和が同じであるという法則をヘスの法則と言い、熱化学方程式を解くうえで非常に大事な法則になります。
一種のエネルギー保存則ですから、物理をやっている人には当たり前に思える事かも知れませんね。
今回はこれでおわりです。次回は、このヘスの法則を用いた熱化学方程式の解き方を説明します。

平野 晃康
株式会社CMP代表取締役
私立大学医学部に入ろう.COM管理人
大学受験アナリスト・予備校講師
昭和53年生まれ、予備校講師歴13年、大学院生の頃から予備校講師として化学・数学を主体に教鞭を取る。名古屋セミナーグループ医進サクセス室長を経て、株式会社CMPを設立、医学部受験情報を配信するメディアサイト私立大学医学部に入ろう.COMを立ち上げる傍ら、朝日新聞社・大学通信・ルックデータ出版などのコラム寄稿・取材などを行う。

