第32回:熱化学方程式②【化学反応と熱の出入り】
熱化学方程式の作り方の例として、黒鉛の燃焼反応を考えてみることにします。黒鉛は炭素のみからなる物質で、燃焼熱は394KJ/molです。
熱化学方程式は、化学反応式の中に放出、あるいは吸収される熱量の情報を入れたものです。ですので、まず化学反応式を書きます。炭素が空気中の酸素と結びついてCO2となる反応ですね。
ここで注意して欲しい事があります。普通、化学反応式では係数が分数になるのはNG です。しかし、熱化学方程式の場合、1molの物質が反応する場合の熱量の出入りですから、その物質の係数が1になるようにします。今回は、黒鉛の燃焼熱を考えるので、黒鉛の係数を1にします。
(炭素の燃焼の化学反応式) C + O2 → CO2
ここに、熱量を加えます。今回は黒鉛1molあたり394KJ ですから、右辺に+394KJ を加えます。
(化学反応式に熱量を加えたもの) C + O2 → CO2 + 394KJ
次に、各物質の状態を加えます、気体のものは(気)、固体のものは(固)、液体のものは(液)、水溶液はaq を物質の後ろに加えます。Cは同素体にダイヤモンドと黒鉛がありますから、C(黒鉛)と書きます。
(各物質の状態を明記したもの) C(黒鉛) + O2(気) → CO2(気) + 394KJ
最後に、→を=に直します。これで、熱化学方程式の完成です。
(炭素の燃焼の熱化学方程式) C(黒鉛) + O2(気) = CO2(気) + 394KJ
注意)反応が吸熱の場合は、熱量の符号が + ではなく-になります。
※黒鉛の燃焼熱が394KJ であるということはC(黒鉛)とO2(気)1molの持っているエネルギーが
CO2(気)の持っているエネルギーより394KJ 多いという事です。
このことは熱化学方程式 C(黒鉛) + O2(気) = CO2(気) + 394KJからも読み取れますね。
黒鉛の燃焼熱が394KJ/molというのを、エネルギー図に表すとどうなるか、確認しておきましょう。黒鉛の燃焼熱が394KJ/mol というのは、C(黒鉛)+O2(気)よりもCO2(気)の方が1mol あたりに持っている化学的エネルギーが394KJ だけ小さいという意味です。
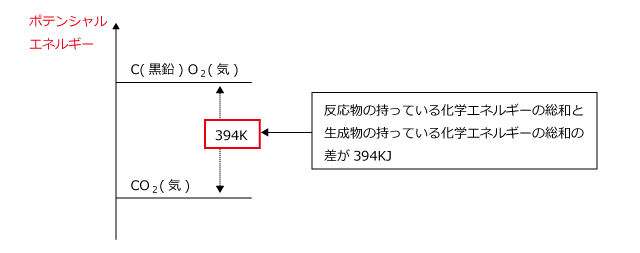
縦軸にエネルギーの大きさを取って図にするとこのような感じになります。上のほうにあるものほど持っているエネルギーが大きいという事を表しています。
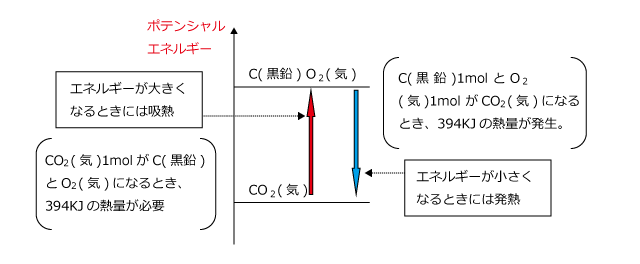
ですから、C(黒鉛)+O2(気)→CO2(気)のときは発熱反応になりますが、CO2(気)→C(黒鉛)+O2(気)の時は吸熱反応になりますね。

平野 晃康
株式会社CMP代表取締役
私立大学医学部に入ろう.COM管理人
大学受験アナリスト・予備校講師
昭和53年生まれ、予備校講師歴13年、大学院生の頃から予備校講師として化学・数学を主体に教鞭を取る。名古屋セミナーグループ医進サクセス室長を経て、株式会社CMPを設立、医学部受験情報を配信するメディアサイト私立大学医学部に入ろう.COMを立ち上げる傍ら、朝日新聞社・大学通信・ルックデータ出版などのコラム寄稿・取材などを行う。

