理論化学
化学講座 第24回:イオン化傾向とイオン化列
以前、金属は電子を放出する性質を持つ元素であることを説明しました。この金属が電子を放出する性質の大きさをイオン化傾向といいます。
イオン化列とイオン化傾向
イオン化傾向の大きなものほど電子を放出して陽イオンになりやすく ( 酸化されやすく ) 反応性の高い金属です。金属をこのイオン化傾向の大きな順に並べたものをイオン化列といい、下表のようになっています。

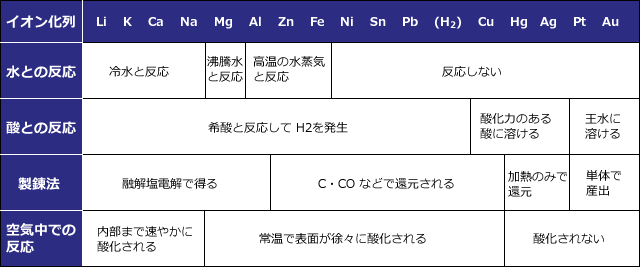
上表は空気や水や酸と各金属の反応ですが、イオン化傾向の大きなものほど激しく反応する事が分かりますね。
例えば、イオン化傾向の大きな Li~Na では空気中の酸素によって内部まで酸化されてしまうのに対して、イオン化傾向の小さな Pt や Au は空気によって全く酸化されません。
この2つめの表は大事ですから、このまま覚えてください。Al よりイオン化傾向の大きなものは融解塩電解で単体を得るという事や水・酸との反応は頻出です。
また、この表は、金属の単体が電子を放出する力の大きさの順を表しています。異なる2 種類の金属を接触させると、表面で電子の押し付け合いが起こり、イオン化傾向の大きい方から小さい方へと電子が流れます。(詳しくは次回、電池の原理を説明するときにお話しします。)
では、イオン化傾向の小さな金属のイオンと、イオン化傾向の大きな金属の単体を接触させたらどうなるでしょうか。
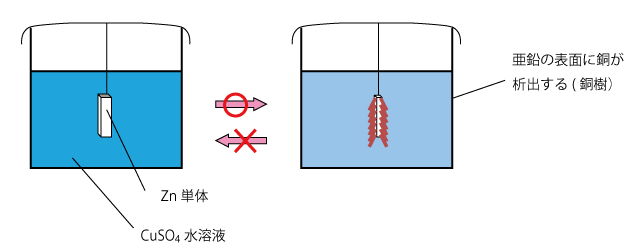
たとえば、硫酸銅水溶液中に、亜鉛の単体を入れると、Zn の方が Cu より電子を押し付ける力が強いため、次のような反応が起こって Zn が溶解して Zn 板の表面に Cu が析出します。

このとき、Cu が小さな枝のように Zn の表面に析出するため、銅樹と呼ばれます。同様の現象は、水溶液が硝酸銀の場合でも起こり、この場合は銀が析出するので、銀樹と呼びます。
このとき、Cu が小さな枝のように Zn の表面に析出するため、銅樹と呼ばれます。同様の現象は、水溶液が硝酸銀の場合でも起こり、この場合は銀が析出するので、銀樹と呼びます。