理論化学
化学講座 第18回:酸と塩基(5)
酸化還元反応の定義(酸素原子のやり取りによる定義)
実は、もともと酸化反応は、その名前の通り酸素原子と物質が結びつく反応として定義されていました。また、還元反応はその逆の反応で、酸素原子が物質から脱離する反応と定義されていました。
では、酸素が結びつくことが酸化反応になるという定義と、電子の授受による定義は矛盾しないのでしょうか。
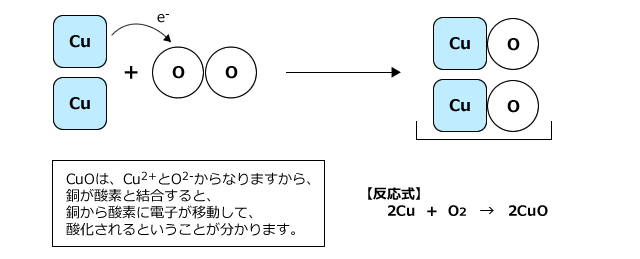
酸素は電気陰性度がフッ素に次いで2番目に大きな元素ですから、物質が酸素原子と結びつくと、物質の持っている電子が酸素原子の方に引き寄せられてしまいます。これは物質が電子を奪われた事に等しいですから、物質が酸素に酸化されたということになるわけです。
逆に、物質から酸素原子が脱離するときには、酸素原子に引き寄せられていた電子が戻ってきますから、物質が還元された事になるのです。

酸化される ・・・ 酸素原子と結びつく反応
還元される ・・・ 酸素原子が脱離する反応
例として、銅をが空気中で加熱すると、銅と酸素が化合して酸化銅が生じる反応を挙げることができます。
そういえば、中学校で習ったと思いますが、金属の酸化物を還元するときには、炭素の粉末を加えて加熱するんでしたね。
これが還元反応であることも、この定義で説明できます。ちょっと確認しておきましょう。

※炭素ではなく、水素でも同様の還元反応をすることができます。この場合、生じるのはH2Oです。