理論化学
化学講座 第33回:熱化学方程式③【熱化学方程式の解き方】
例題) 次の熱化学方程式を利用して、C2H5OH(液)の生成熱を求めよ。
C(黒鉛) + O2(気) = CO2(気) + 394KJ・・・・①
H2(気) + O2(気) = H2O(液) + 286KJ・・・・②
C2H5OH(液) + 3O2(気) = 2CO2(気) + 3H2O(液) + 1370KJ・・・・③
●代数的な熱化学方程式の解法のポイント
Qを含む熱化学方程式を書き、そこにある化合物を他の反応式を利用して単体と熱量に書き換える。全ての化合物を単体に書き換えると、両辺の単体がきれいに打ち消し合って、熱量のみの式になる。
解説・解答)
まず、求めたい熱量をQKJ/molとしてQを含む熱化学方程式を書きます。今回求めたいのはエタノールの生成熱です。生成熱は物質が単体から生じるときに放出する熱量ですから、熱化学方程式は下式のようになります。
2C(黒鉛) + 3H2(気) + O2(気) = C2H5OH(液) + QKJ・・・・④
ここまでは先ほどと同じです。次に、ここにある物質のうち、O2以外の物質を消すため、①~③式を変形します。
③式より、C2H5OH(液) = 2CO2(気) + 3H2O(液) - 3O2(気) + 1370KJ
これを④式に代入します。
2C(黒鉛) + 3H2(気) + O2(気)= (2CO2(気) + 3H2O(液) - 3O2(気) + 1370KJ) + QKJ ・・・・④′
今度は、CO2(気) と H2O(液)という二種類の化合物が出てきましたので、①式と②式を変形して、これを単体のみの式に書きなおします。
①式より、CO2(気) =C(黒鉛) + O2(気) - 394KJ
②式より、H2O(液) = H2(気) - O2(気) - 286KJ
これらを④′式に代入します。
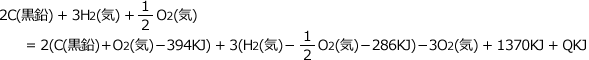
これを整理すると、両辺の単体が全て消えて、熱量だけの方程式が得られます。
0 = 2×(-394) + 3×(-286) + 1370 + Q KJ
これを解くと、Q = 276 KJ よって、エタノールの生成熱は276KJ/mol
さて、どうでしたか。今回は熱化学方程式の解き方を2パターンやってみました。
両方とも、やり方をしっかり理解してください。この解き方を理解すれば、応用問題もちゃんと解けるようになります。