理論化学
化学講座 第35回:単体と化合物、純物質と混合物、分離と精製
さて、混合物は単にいくつかの純物質が混ざっただけのものですから、適当な処理を施す事によって純物質に分けることができます。この操作を分離といい、分離を繰り返して純度を高める事を精製といいます。
ですから、分離と精製の操作は同じです。次の7種類の分離の方法を覚えておきましょう。
- ろ過 : ろ紙を用いて、固体と液体を分離する
- 蒸留 : 2種類以上の液体の沸点の差を利用して分離する
- 分留 :いかなる濃度でも共沸しない2種類以上の液体の沸点の差を利用して分離する。高校化学では液体空気と石油に用いる。
- 再結晶 : 温度による溶解度の差を利用して分離する
- 抽出 : 溶媒に対する溶解度の差を利用して分離する
- 昇華 : 昇華性の物質と、昇華性の無い物質を分離する
- クロマトグラフィー : ろ紙やカラムへの吸着力の差を利用して分離する
(1) ろ過(液体と固体の混合物から、固体をろ紙でこしとって分離する)
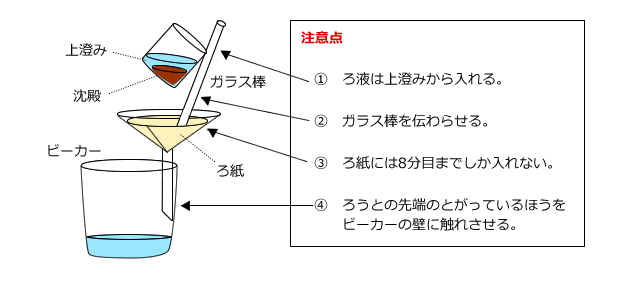
ろ過は、ろ紙を用いて液体と液体に溶けていない沈殿(固体)を分離する方法です。例えば、砂と水の混合物(簡単に言うと泥水)から砂を取り出す場合や、生成した沈殿を取り出す場合には、ろ過を用います。
(2) 蒸留(沸点の違いに着目して分離する)
蒸留は、沸点の違いにより分離する方法です。例えば、水とエタノールの混合物を蒸留で分離するためには、下図のような装置を用いて蒸留を行います。

(3) 分留(沸点の違いに着目して分離する)
分留というのは分別蒸留の略称です。蒸留と何が違うの、という事を聞く人も多いのですが、分留は蒸留の一種で、共沸点の無い混合溶液の場合に用います。
共沸点というのは、溶液と蒸気の組成が全く同じになる温度の事で、この温度に達すると、それ以上蒸留で分離・精製をすることができません。しかし、この共沸点が無い溶液は、蒸留によって完全に成分に分離することができるのです。
高校化学でよく出てくるのは石油と液体空気の分留ですね。